Önemli Bilgiler
Belediye İle İlgili İşlemler
Eczane sahip ve mesul müdürü olan eczacılar yeni eczane açılışlarında mahallin bağlı bulunduğu belediyeye “İlan ve reklam vergisi” ve “Çevre temizlik vergisi” için müracaat etmek zorundadır.
“İlan ve reklam vergisi” için ilgili belediyeden temin edilecek olan matbu form'a ; tabelanın özellikleri yazılacak ve kullanılan boya vs.nin faturası ibraz edilecektir. Daha sonraki senelerde eski makbuzları ile birlikte nisan ve ekim ayları içinde (iki eşit taksitte) belediyeye tekrar müracaat edilecektir.
İşyeri Açma Ruhsatı için Gerekli Belgeler (Sarıçam ve Yüreğir Belediyeleri için)
SIHHI İŞYERİ İÇİN GEREKLİ EVRAK LİSTESİ
1-Tapu senedi-tapu sahibinin kimlik fotokopisi
2-Yapı kullanım izin belgesi (Bina 12 Ekim 2004 tarihinden önce yapılmış ise izin belgesine gerek yok. Bu konuda Yüreğir Belediyesi Emlak Müdürlüğü beyan dökümünden bilgi alınabilir.)
3-İşyeri tapu sahibine ait değilse, kira kontratı veya muvafakat name
4-Vergi levhası
5-Ruhsat fotokopisi
6-İmza beyanı
7-Oda kayıt ve faaliyet belgesi
8-Kimlik fotokopisi(Vatandaşlık numaralı)
9-İtfaiye raporu (Büyükşehir Belediyesinden)
10- Plastik telli dosya
30.12.2016
Oda Denetçi Eczacılarının Eczane Denetiminde Aradıkları Hususlar
- Eczacının işinin başında olup olmadığı ?
- Çalışma saatlerinde beyaz önlük giyip giymediği, isimlik kullanıp kullanmadığı ?
- Eczanenin ruhsatının olup olmadığı ?
- Eczanenin ortamının hijyenik koşullara uygun olup olmadığı ?
- Eczane raflarında son kullanma süresi dolmuş ilaç bedelsiz numune, SSK ilacı, küpürü kesik ilaç yada sürşarj genelgesine aykırı , etiketli ilaç bulunup bulunmadığı ?
- Soğuk zincir koşullarında saklanması ilaçların eczanede buzdolabında bulunup bulunmadığı ve bu tür ilaçların dağıtımında Sağlık Bakanlığının genelgesi doğrultusunda soğuk zincir koşullarına uyulup uyulmadığı ?
- Eczanede bulunan ilaçların saklandığı ortam koşullarının (ısı, ışık, nem vb noktalarda) olup olmadığı ?
- Eczanede bulundurulması gerekli defterlerin bulunup bulunmadığı ?
- Eczanede majistral tarifenin bulunup bulunmadığı ?
- Yasa dışı yollara giren ilaçların eczanede satılıp satılmadığı ?
- Eczanede ışıklı nöbet levhası bulunup bulunmadığı ?
- Nöbetçi eczane kartlarının doğru asılıp asılmadığı ve bu kartlardaki nöbetçi eczane bilgilerinin eksiksiz olup olmadığı ?
- Eczacı odası yönetim kurulunca belirlenen eczane çalışma saatlerine ve tatillerine uyulup uyulmadığı ?
- Eczane tanıtım levhalarının 6197 sayılı yasaya bağlı olarak hazırlanan yönetmelik hükümlerine uygun olmadığı ?
- Eczane vitrininde eczacı odalarınca onaylanmış afişlerin dışında (deontolojiye aykırı) ticari rekabete dayalı duyuru ve ilaç tanıtım yönetmeliğine aykırı; halka yönelik ilaç firmalarınca dağıtılan reklam ( tanıtım) afişi olup olmadığı eczane vitrininde ışıktan korunması gereken ürünlerin bulundurulup bulundurulmadığı ?
- Resmi ve özel kurum .kuruluşlara Büyük Kongre kararı dışında (%5’i aşan iskonto yapılmadığı ,yasa gereği alınması gereken hasta katılım payının eksiksiz alınıp alınmadığı ?
- Kamuoyunda eczacıları ve eczacılık hizmetlerini olumsuz etkileyen reçete toplama ,çırak ikili anlaşma ,telefon ve faksla sipariş alma vb.) uygulamaların olup olmadığı ?
- Eczanede yasa yönetmelik ve genelgelere aykırı (malzeme ürün v.b) satış yapılıp yapılmadığı ?
30.12.2016
Sağlık Müdürlüğünün Eczane Denetiminde Aradıkları Hususlar (2016)
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
* Eczanede sunulan hizmetin kalitesinin arttırılması, eczacılık hizmetinin hastaya bizzat eczacı tarafından sunulmasının temini ve güvenliğin sağlanması gerekçesiyle tavsiye niteliğindedir
30.12.2016
Nasıl Bağ-Kur'lu olunulur?
1479 sayılı esnaf ve sanatkarlar ve diğer baımsız çalışanlar Sosyal Sigortalar Kanunu( Bağ-Kur Kanunu) ,( Sayı:1479 Kanun tadil no 2249),( Resmi gazete yayın tarihi:04,05,1979) na göre eczane sahip ve mesul müdür olan eczacılar Bağ-Kur sigortalısı olmak durumundadırlar.
Bağ-Kur’ lu Olmanın Başlangıç Tarihi
1479 sayılı kanunun 3165 sayılı kanunla değişik “kanun amacı, sigortalı sayılanlar ve sayılmayanlar” başlıklı 24 maddesi ile “Sigortalının başlangıç ve bitiş tarihi” başlıklı 25. Maddesinin uygulanması ile ilgili olarak Bağ-Kur yönetim kurulunun 21,07,1995 tarih ve 93/1/193 sayılı kararı gereği ; Gelir vergisi mükellefiyetlerinin başladığı tarihten önce meslek kuruluşu kaydı olanların, bu sürelerde kendi nam ve hesabına bağımsız, çalışması olmadığını meslek kuruluşlarından belgelemeleri halinde sigortalkları gelir vergisi mükellefiyetlerinin başladığı tarihten başlatılacak ; gelir vergisi mükellefiyetlerinin sona erdiği tarihten sonra meslek kurulup kaydi devam edenlerin Bu sürelerde kendi nam ve hesabına bağımsız çalışması olmadığı meslek kuruluşlarından belgelemeleri halinde sigortalıkları gelir vergisi mükellefiyetleri sona erdiği tarih itibari ile sona erecektir.
Bağ-Kur’ a Başvuru
Sigortalı sayılan eczacılar, sigortalı sayıldıkları tarihten itibaren en geç üç ay içinde “Bağ-Kur a giriş bildirgesi”nin bölge eczacı odasyna onaylattırıldığı tarih başvuru tarihi sayılır ve bu tarih “basamak” tesbitinde esas alınır.
Re’sen Tescil
Bağ-Kur kanununa göre sigortalı sayılanlar, sigortalı sayıldıkları tarihten itibaren 3 ay içinde Bağ-Kur il müdürlüklerine veya vergi dairelerine veyahut ilgili diğer kuruluşlara tescillerini yaptırmazlarsa; ilgili yerlerden alınacak bilgi ve belgelere dayanılarak tescilleri Bağ-Kur tarafından re’ sen yapılır.
30.12.2016
SGK Sözleşme İşlemleri
Eczacı tarafından ilk kez sözleşme imzalama halinde eczacıya ait;
- Kimlik fotokopisi (T.C Kimlik No ile birlikte),
- Ruhsat fotokopisi,
- İmza sirkülerinin noter onaylı örneği,
- Eczacı odasından alınan yeni tarihli “Sözleşmeye Engel Yoktur” belgesi,
- Eczacının sosyal güvenlik durumunu gösterir belge,
- Mükellefin bağlı olduğu vergi dairesinden onaylı form (SUT eki EK-3/B)
- Bölge Eczacı Odasından onaylı sözleşme metni,
Yenileme halinde;
- Bölge Eczacı Odasından onaylı sözleşme metni
- Mükellefin bağlı olduğu vergi dairesinden onaylı form (SUT eki EK-3/B)
-Ruhsat fotokopisi (Değişiklik olması halinde)
- Eczacı odasından alınan yeni tarihli “Sözleşmeye Engel Yoktur” belgesi,
Kuruma bir dilekçe ekinde ibraz edilecektir.(Dilekçe Örneği)
30.12.2016
Maliye Bakanlıgı ve Yeşil Kart Sözleşme İşlemleri
Eczacı tarafından ilk kez sözleşme imzalama halinde eczacıya ait;
- Kimlik fotokopisi (T.C Kimlik No ile birlikte),
- Ruhsat fotokopisi,
- İmza sirkülerinin noter onaylı örneği,
- Eczacı odasından alınan yeni tarihli “Sözleşmeye Engel Yoktur” belgesi,
- Eczacının sosyal güvenlik durumunu gösterir belge,
- Mükellefin bağlı olduğu vergi dairesinden onaylı form (SUT eki EK-3/B)
- Bölge Eczacı Odasından onaylı sözleşme metni,
Yenileme halinde;
- Bölge Eczacı Odasından onaylı sözleşme metni
- Mükellefin bağlı olduğu vergi dairesinden onaylı form (SUT eki EK-3/B)
-Ruhsat fotokopisi (Değişiklik olması halinde)
- Eczacı odasından alınan yeni tarihli “Sözleşmeye Engel Yoktur” belgesi,
Kuruma bir dilekçe ekinde ibraz edilecektir.
30.12.2016
KOSGEB Girişimcilik Destek Programı

KOSGEB ZONGULDAK MÜDÜRLÜĞÜ
Çaydamar Mah. Ahmet Taner Kışlası Cad. No:7 Merkez/ZONGULDAK
Eposta:zonguldak@kosgeb.gov.tr
Tel:0372 253 36 48
Fax:0372 253 67 49
Karadeniz Ereğli TSO - KOSGEB Temsilciliği
MÜFTÜ MAHALLESİ-MEYDANBAŞI CAD. ÇAMLIK SOKAK NO 9 KRDZ.EREĞLİ / ZONGULDAK
Eposta:
Tel:0372 316 11 61
Fax:0372 316 88 97
KOSGEB BARTIN MÜDÜRLÜĞÜ
Aşağıdüz Mevkii Toptancılar Sitesi No: 19-1 Gecen
Eposta:bartin@kosgeb.gov.tr
Tel:03782200409
Fax:03782200412
Girişimcilik DestekProgramınınAmacı
- Girişimciliğin desteklenmesi
- Girişimciliğin yaygınlaştırılması
- Başarılı işletmelerin kurulması
Programdan Kimler Yararlanabilir?
- Küçük ve Orta Ölçekli İşletmeler(31/12/2017’e kadar),
- Girişimciler
- İşletici Kuruluşlar (İş Geliştirme Merkezi’ni yönetmek üzere kurulan tüzel kişilik)
Programın Kapsamı
Bu program,
A.Uygulamalı Girişimcilik Eğitimi,
B.Yeni Girişimci Desteği,
C.İş Geliştirme Merkezi (İŞGEM) Desteği
D.İş Planı Ödülünden oluşur.
- A) Uygulamalı Girişimcilik Eğitimi
Uygulamalı Girişimcilik Eğitimleri, ülkede girişimcilik kültürünün yaygınlaştırılması ve başarılı işletmelerin kurulması genel hedefine uygun olarak; girişimcilerin iş kurma ve yürütme konularında bilgi ve beceri sahibi olmaları, bu süreçte kendi rol ve sorumluluklarının farkına varmaları ve kendi iş fikirlerine yönelik iş planı hazırlayabilecek bilgi ve deneyim kazanmaları amacıyla düzenlenir.
Uygulamalı Girişimcilik Eğitimleri;
- KOSGEB birimleri tarafından düzenlenen,
- Ulusal veya uluslararası projeler kapsamında, KOSGEB tarafından yürütülen,
- KOSGEB ile işbirliği içerisinde çeşitli kurum ve kuruluşlar tarafından düzenlenen eğitimler,
- Üniversiteler tarafından örgün eğitim kapsamında verilen girişimcilik dersleri’dir.
Uygulamalı Girişimcilik Eğitimleri, en az 32 saat süren, genel katılıma açık veücretsizeğitimlerdir.
B) Yeni Girişimci Desteği
Destekten Kimler Yararlanabilir?
Bu destekten Uygulamalı Girişimcilik Eğitimini tamamlayan ya da İŞGEM’de yer alacak Girişimciler yararlanabilir.
Girişimcinin başvuru tarihi itibariyle son 1 (bir) yıl içerisinde aynı faaliyet konusunda (Güncel NACE-Ekonomik Faaliyet Sınıflamasında yer alan 4’lü koda göre) şahıs işletmesinin bulunmaması gerekmektedir. Ayrıca Girişimcinin tüzel kişi statüsünde kurulmuş herhangi bir işletmede%50’den fazla ortaklığının olmaması gerekmektedir.
Girişimcinin kuracağı işletme, Türk Ticaret Kanunu’nda tanımlı gerçek veya tüzel kişi statüsünde olmalıdır.
Girişimcinin destek sürecinde; başka bir işletme/kurum/kuruluşta SGK hükümlerine tabi olarak çalışmaması gerekmektedir. Ancak İnkübatör’lerde yer alacak öğretim elemanları için bu şart aranmaz.
Destek Unsurları Nelerdir?
|
DESTEK UNSURU |
|
ÜST LİMİTİ (TL) |
DESTEK ORANI (%) (1. ve 2.Bölge) |
DESTEK ORANI (%) (3., 4., 5. ve 6. Bölge) |
|
İşletme Kuruluş Desteği |
Geri Ödemesiz |
2.000 |
- |
|
|
Kuruluş Dönemi Makine, Teçhizat, Ofis Donanım ve Yazılım Desteği |
18.000 |
60 Kadın Girişimci, Gazi, Birinci derecede şehit yakını veya Engelli |
70 Kadın Girişimci, Gazi, Birinci derecede şehit yakını veya Engelli |
|
|
İşletme Giderleri Desteği |
30.000 |
|||
|
Geri Ödemesiz Destekler Toplamı |
50.000 |
|||
|
Sabit Yatırım Desteği |
Geri Ödemeli |
100.000 |
||
(1) İşletme kuruluş giderleri için geri ödemesiz olarak 2.000 (iki bin) TL destek sağlanır.
(2) Kuruluş Dönemi Makine, Teçhizat, Ofis Donanım ve Yazılım Desteği kapsamında, işletmenin kuruluş tarihinden itibaren 24 (yirmi dört) ay içinde satın alınan/alınacak makine, teçhizat, yazılım ve ofis donanımları için geri ödemesiz olarak üst limiti 18.000 (on sekiz bin) TL destek sağlanır.
(3) İşletme Giderleri Desteği kapsamında, işletme kurluştarihinden itibaren 24 (yirmi dört) ay içinde gerçekleşen işyeri kirası ve personel net ücretlerine yönelik olarak, aylık azami 5.000(beş bin) TL ve toplamda geri ödemesiz olarak 30.000 (otuz bin) TL destek sağlanır.
(4) Kuruluş Dönemi Makine, Teçhizat, Yazılım ve Ofis Donanım Desteği ile İşletme Giderleri Desteği üst limitleri; bu destek unsurları için belirlenen üst limitlerin toplamını aşmamak üzere ihtiyaç duyulması halinde Kurul Kararı ile % 50 (elli)’ye kadar arttırılabilir. Bu durumda Kuruluş Dönemi Makine, Teçhizat, Yazılım ve Ofis Donanım Desteğinin üst limiti 27.000 (yirmi yedi bin) TL, İşletme Giderleri Desteği üst limiti 45.000 (kırk beş bin) TL ve her iki desteğin üst limitleri toplamı ise 48.000 (kırk sekiz bin) TL’yi geçemez.

(5) Sabit Yatırım Desteği kapsamında, işletme kuruluş tarihindenitibaren 24 (yirmi dört) ay içinde satın alınacak makine, teçhizat ve yazılım için teminat karşılığı geri ödemeli olarak 100.000 (yüz bin) TL destek sağlanır.
Girişimcilik Destek Programı Uygulama Esasları
Uygulamalı Girişimcilik Eğitimi Duyuruları
07.01.2017
Eczanelerde Bulundurulması Zorunlu İlaçlar (ESKİ LİSTE)
- Aminofilin enj.
- Antihistaminik enj.
- Oksijenli su
- Diazepam tab.
- Digoksin enj.
- Fenobarbital tab.
- Furosemide enj.
- Insülin kristalize enj.
- Insülin nph
- Isosorbit dinitrat sublingual tab.
- Kortikosteroid enj.
- Klonozepam tab.
- Klorpromazin enj.
- Kalsiyum enj.
- Nifedipin tab.
- Nitrogliserin tab./sprey
- Trimetobenzamid enj.
Büyük Hacimli Paranteral Solüsyonlar
- %0,9 izotonik sodyum klorür
- %5 dekstroz solüsyonu
- Multipl eloktrolid solüsyonu
- Dekstran 40/70
Eczanelerde Bulundurulması Zorunlu Tıbbi Malzeme
- Beden derecesi
- Branül
- Elastik bandaj
- Flaster
- Kelebek set
- Sarg? bezi
- Serum seti
- Steril gaz kompres
- Steril enjektör (tek kullanımlık)
- Sonda (kadın erkek en az 3 değişik numara)
08.01.2017
Yurt Dışından İlaç Temini
Yurt Dışından İlaç Temini Birimi; T.C. Sağlık Bakanlığı ile Türk Eczacıları Birliği arasında yurt dışından ilaç teminine ilişkin yapılan protokol çerçevesinde ilaç ithal eden iktisadi bir kuruluştur.
Amaç; hastaların tedavisi için hekim tarafından gerekli görülerek reçeteye yazılan, ancak Türkiye’de ruhsatlı olmayan veya ruhsatlı olduğu halde çeşitli nedenlerle üretimi veya ithalatı yapılamayan ve T.C. Sağlık Bakanlığı’nca ithalat izni verilen reçete muhteviyatı ilaçları ithal edip iyi dağıtım kurallarına uygun olarak hasta/hasta yakınına teslim etmektir.
TEB Yurtdışından İlaç Temini Hasta ve Eczacı Bilgilendirme Broşürü
Yurtdışından İlaç Temini Ön Kontrol Paneli Kullanım Kılavuzu
Yurtdışından İlaç Temini Hizmet Bedeli Fatura Örneği
İthal ilaç işlem sürecindeki ilacınız hakkında sorgulama yapmak için tıklayın.
BAŞVURU PROSEDÜRÜ
İSTENİLEN BELGELER:
SOSYAL GÜVENLİK KURUMU MENSUBU HASTALAR İÇİN:
1- Reçetenin aslı
2- İlaç kullanım raporunun fotokopi örneği
3- İlaca bağlı Sosyal Güvenlik Kurumunca istenen diğer evraklar
4- Hasta Bilgi Formu (Hasta Bilgi Formu İçin Tıklayınız.)
TÜRKİYE İŞ BANKASI VE YAPI KREDİ BANKASI MENSUBU HASTALAR İÇİN:
1- Reçetenin aslı
2- İlaç kullanım raporunun fotokopi örneği
3- Hastanın/Hak sahibinin banka mensubu olduğunu gösterir belge
4- Hasta Bilgi Formu (Hasta Bilgi Formu İçin Tıklayınız.)
REÇETE BEDELLERİNİ KENDİLERİ ÖDEYECEK HASTALAR İÇİN:
1- Reçete (Fax yolu ile gönderilebilir)
2- İlaç bedelinin banka hesaplarımızdan birine yatırıldığına dair dekont (Fax yolu ile gönderilebilir)
*İlaç bedellerinin hasta adına yatırılması esnasında dekontun açıklama kısmına hasta adı ve TC kimlik numarasının mutlaka yazdırılması gerekmektedir.
3- Hasta Bilgi Formu (Fax yolu ile gönderilebilir) (Hasta Bilgi Formu İçin Tıklayınız.)
REÇETE VE İLAÇ KULLANIM RAPORLARINDA DİKKAT EDİLMESİ GEREKEN HUSUSLAR:
| 1 | Yurt dışından ilaç temini için öncelikli şart T.C. Sağlık Bakanlığı Türkiye İlaç ve Tıbbi Cihaz Kurumu’nun ithalat için onay vermesidir. Bu onaydan muaf olan ilaç ve endikasyonları Kurum tarafından yayınlanmaktadır. Türkiye İlaç ve Tıbbi Cihaz Kurumu tarafından yayınlanan Yurtdışı Aktif İlaç Listesi için tıklayınız |
| 2 | Aslı gibidir onayı; reçeteyi yazan doktor tarafından veya raporu çıkaran hastanedeki doktorlardan biri tarafından veya raporun aslı Birliğimize iletildiği takdirde eczacılarımız tarafından yapılabilir. |
| 3 | İlaç kullanım raporunda verildiği hastanenin açık adı bulunması zorunludur. |
| 4 | Hasta adı, soyadı ve TC Kimlik numarası reçete ve ilaç kullanım raporu ile uyumlu olacaktır. |
| 5 | Raporda TC Kimlik numarası mutlaka yer alacaktır. |
| 6 | Raporda raporun tarih ve numarası mutlaka yer alacaktır. |
| 7 | Reçete tarihi, rapor tarihi ile aynı veya o tarihten sonraki bir tarih olmalıdır. Reçete tarihi rapor tarihinden önce olamaz. |
| 8 | Sağlık kurulu raporlarında 3 uzman hekim, tek hekim raporlarında ise 1 uzman hekim kaşe ve ıslak imzası aranmaktadır. |
| 9 | Reçetede, tarih, protokol numarası, tanı, ilaç adı, kullanım dozu, kutu adedi (yazı ve rakam ile) mutlaka yazılmış olacaktır. Reçete üzerinde herhangi bir karalama veya düzeltme yapılması ihtiyacı halinde, düzeltme yapılan yere reçeteyi yazan hekim, kaşesini basarak ıslak imza atmalıdır. |
| 10 | Reçetede, reçeteyi yazan uzman hekimin kaşe ve imzası (Kaşede uzman olduğunu gösterir ve diploma numarası okunabilir olmak kaydıyla) mutlak surette bulunacaktır. Hekimin reçete, rapor ve eklerindeki imzaları (paraf şeklinde olmayacaktır) arasında uyum aranmaktadır. |
Yurt Dışından İlaç Temini Birimi Merkez
Cinnah Cad. Willy Brandt Sok. No:9
Çankaya/ANKARA
Telefon: 0312 409 81 81
Faks: 0312 409 81 13
Reçete Bedellerini Kendileri Ödeyecek Hastalar İçin Faks: 0312 409 81 74
E-posta: ithalilac@teb.org.tr
Yurt Dışından İlaç Temini Birimi İstanbul Şubesi
Millet Caddesi No:109/A Fatih İSTANBUL
Çapa Hastanesi Kan Bankası Kapısı Karşısı
Telefon: 0212 459 10 00
Faks: 0212 589 19 15
Yurt Dışından İlaç Temini Birimi İstanbul 2. Şubesi
Topkapı Mahallesi Turgut Özal(Millet) Caddesi NO: 154/A Çapa/Fatih/İSTANBUL
Telefon: 0212 459 10 00
Faks: 0212 523 23 88
E-posta: ithalilac@teb.org.tr
Yurt Dışından İlaç Temini Birimine Mesaj Göndermek İçin Tıklayınız.
Hasta Memnuniyeti Anketi için tıklayınız.
19.01.2017
Ölçü ve Tartı Aletlerinin Kalibrasyon İşlemleri Hakkında (2017)

Tartı aletlerinin periodik muayenelerinin 2 (iki) yılda bir yapılması yasal zorunluluktur.Süresi dolan tartı aletlerinin periodik muayenesinin yapılarak damgalanması gerekmektedir. Bu işlem için son başvuru tarihi28 Şubat 2017Salıgünü mesai bitimine kadardır.
4 Eylül 2013 tarihli resmi gazetede yayınlanan tartı aletleri muayene yönetmeliği’nin 8.maddesi ile; eczanelerde kullanılan tartı aletlerinin gramlar hariç olmak üzere periyodik muayeneleri yetkili muayene servislerine verilmiştir.
Gram takımlarının(kütle setleri) muayene yetkisi iseİl Bilim Sanayi ve Teknoloji Müdürlüğü’ndedir.
29 Aralık 2016 Tarih ve 29933 Sayılı Resmi Gazetede belirtilen Kütle setleri (bütün Sınıflar için) 2017Muayene ve Damga ücreti 52.40 TLdir. Muhasebe veya Mal Müdürlüğü hesabına 600 - 03.01.02.13 koduyla 52.40 TL yatırılarak Bilim Sanayi ve Teknoloji İl Müdürlüğüne(Zonguldak Bilim Sanayii ve Teknoloji İl Müdürlüğü Valilik Binası 4. Kat 401 nolu oda), ( Bartın Bilim Sanayi ve Teknoloji İl Müdürlüğü Bartın Valiliğinde)dekont ile başvurular yapılacaktır.
Ölçü ve tartı aletlerinin kalibrasyon işlemleriile ilgili Zonguldak ve Bartın İllerindeDenge Tartı AletleriYetkili muayene servisi ile yapılan görüşmelerde Terazilerin Kalibrasyon başvurusu ve Kontrollerinin aynı andaeczanelerde 57 TL (KDV Dahil)karşılığı yapılacak, ve faturası ilgili firma tarafından eczacıya teslim edilecektir.
Bu işlem sonunda Ölçü ve Tartı aletleri kalibrasyon belgeleri Denge Tartı Aletleri yetkili muayene servisi tarafından verilecektir.
e-mail: info@dengetartialetleri.com
Telefon: 0 532 113 26 63
07.02.2017
İlave İstihdam Teşviki
“İstihdam Sizden, Sigorta ve Vergi Bizden”
31.12.2017 tarihine kadar özel sektör işverenlerine mevcut çalışanlarına ilave alacakları her bir sigortalı için sigorta ve vergi yüklerini biz üstleniyoruz. İşverenlere ilave istihdam ettikleri sigortalı için 773 TL tutarındaki prim ve vergi yükümlülükleri devlet tarafından karşılanacak.
4447 Sayılı Kanun'un Geçici 17. Maddesi'nde yer alan istihdam teşviki uygulamasına ilişkin sorularınızın cevapları:
Teşvikten Kimler Yararlanmaktadır?
İşveren tarafında: Özel sektör işyerleri yararlanabilir.
İş arayan tarafında: işe alındığı tarihten önce İŞKUR kaydı olan ve son 3 ay içerisinde işsiz olanlar yararlanabilir.
Teşvikten Yararlanma Koşulları Nelerdir?
- Teşvikten yararlanacak işverenin 01.02.2017 tarihinden sonra işe aldığı kişinin, İŞKUR kaydının olması ve 2016 yılı Aralık ayına ilişkin aylık prim ve hizmet belgelerindeki sigortalı sayısına ilave olarak çalıştırılması,
- Aylık prim ve hizmet belgesinin yasal süresi içinde SGK’ya verilmiş olması,
- İşveren tarafından ödenmesi gereken sigorta priminin tamamının yasal süresi içinde ödenmesi,
- İşyerinin SGK’ya yasal ödeme süresi geçmiş sigorta primi, işsizlik sigortası primi, idari para cezası ve bunlara ilişkin gecikme cezası ve gecikme zammı borcunun bulunmaması gerekmektedir.
Teşvikten Hangi Tarihe Kadar Yararlanabiliriz?
Teşvik uygulaması 31.12.2017 tarihinde sona erecektir.
2017 Yılında Açılan İşyeri Sahipleri Yararlanabilecekler mi?
Evet, 2017 yılında yeni tescil yapılan işverenler de teşvikten yararlanabilecektir.
İşveren Her Çalışanı İçin Yararlanabilecek mi?
2016 yılı Aralık ayına ilişkin aylık prim ve hizmet belgelerindeki sigortalı sayısına ilave olarak aldıkları, işe alındığı tarihten önce İŞKUR’a kayıtlı olan her çalışanı için yararlanabilir.
Teşvik Miktarı Ne Kadardır?
Yeni işçi başına verilecek teşvik, mevcut çalışana ilave alınacak her bir sigortalı için asgari ücret üzerinden prim ve vergi yükümlülükleri (773 TL) kadardır.
Söz Konusu Teşvikten Yararlanan İşverenler Diğer Teşviklerden Yararlanabilir Mi?
İşverenlerimiz bu teşvike konu olan sigortalı için aynı dönemde diğer sigorta primi teşvik, destek ve indirimlerinden yararlanamayacaklardır. Ancak bu teşvik harici teşviklerden diğer çalışanları için yararlanma hakları bulunmaktadır.
İşverenin Teşvikten Yararlanmak İçin Nereye Başvurması Gerekmektedir?
Destekten yararlanabilmek için işverenlerin e-Bildirge kanalıyla başvuruda bulunması gerekmektedir. Kapsama giren sigortalılara ilişkin e-Bildirge kanalıyla İşverenlerce yapılacak başvurular, www.sgk.gov.tr adresinden e-Bildirge sistemi üzerinde “4447 / Geçici 17. Madde İşveren Desteği” menüsü işaretlenmek suretiyle erişilen ekran vasıtasıyla yapılmaktadır.
09.03.2017
Kadın, Genç ve Mesleki Yeterlilik Teşviki
Tarihler: 01.03.2011 - 31.12.2020
A) 18-29 yaş arası erkekler ile 18 yaşından büyük kadınlardan;
- Mesleki yeterlik belgesine sahip olanlar 48 ay süreyle,
- Mesleki ve teknik eğitimi tamamlayanlar veya işgücü yetiştirme kurslarını bitirenler 36 ay süreyle,
- Hiçbir belge veya niteliğe sahip olmayanlar 24 ay süreyle,
B) 29 yaşından büyük erkeklerden;
- Mesleki yeterlik belgesine sahip olanlar ile mesleki ve teknik eğitimi tamamlayanlar veya işgücü yetiştirme kurslarını bitirenler 24 ay süreyle,
C) Çalışmakta iken;
- 01.03.2011 tarihten sonra mesleki yeterlik belgesi alanlar, mesleki ve teknik eğitimi tamamlayanlar veya işgücü yetiştirme kurslarını bitirenler için 12 ay süreyle,
D) Yukarıda (A), (B), (C) numaralı bentlerde sayılanların İŞKUR’a kayıtlı işsizler arasından alınmaları halinde, öngörülen sürelere ilave olarak 6 ay daha,
E)18 yaşından büyüklerden hiçbir mesleki belge veya niteliğe sahip olmayanların, İŞKUR’a kayıtlı işsizler arasından işe alınmaları halinde 6 ay süreyle, teşvik verilmektedir.
Sigortalıların sahip oldukları mesleki yeterlik, mesleki ve teknik eğitim veya işgücü yetiştirme kurslarına ilişkin belgelerde belirtilen meslek ya da alanlarda işe alınmaları ve/veya çalışıyor olmaları gerekmektedir.
Destekten bir kez yararlanılması ve hak sahipliği süresi tamamlanmadan işsiz kalınması halinde, kalan süreden yeniden yararlanılamaması, ancak daha üst düzeydeki belgelerin temin edilmesi halinde ikinci hak sahipliğinin oluşması, bu durumda ilk hak sahipliğinin süresinin, ikinci hak sahipliğinin süresinden düşülmesi öngörülmektedir.
Kadın, Genç ve Mesleki Yeterlilik Teşviki
09.03.2017
İşbaşı Eğitim Programı Teşviki
Tarihler:01.07.2015 - 31.12.2017
Koşullar:
Teşvikten yararlanmak için:
- 18 yaşından büyük, 29 yaşından küçük olmak.
- 31.12.2017 tarihine kadar başlatılan işbaşı eğitim programlarını tamamlamak.
- Programın bitiminden sonra en geç 3 ay içerisinde programı tamamladıkları meslek alanında istihdam edilmek.
- İşe alındıkları yıldan bir önceki takvim yılında işyerinden bildirilen aylık prim ve hizmet belgelerindeki sigortalı sayısının ortalamasına ilave olmak.
İşe alındıkları işyerinin faaliyet gösterdiği sektör;
- İmalat sanayinde ise 42 ay,
- Diğer sektörlerde ise 30 ay,
sigorta primlerinin işveren hisselerine ait tutarı İşsizlik Sigortası Fonu'ndan karşılanıyor.
30 yaşından büyüklerin istihdam edilmesi durumunda
Katılımcının cinsiyetine göre 6 aydan 30 aya kadar işveren sigorta primi İŞKUR tarafından karşılanmaktadır. (4447 sayılı Kanun Geçici 10.madde)
Ayrıca, Programa katılan kişilere İŞKUR’un yaptığı ödemeler dışında programın düzenlendiği işveren tarafından yapılan ve aylık asgari ücretin yarısını geçmeyen fiili ödemelerin gelir vergisi kanunu gereğince vergi matrahından indirilmesi imkânı bulunmaktadır. (193 sayılı Gelir Vergisi Kanunu 40/11.madde)
İşbaşı Eğitim Programı Teşviki
09.03.2017
Yurt Dışından İlaç Temini Ve Kullanımı Kılavuzu
YURT DIŞINDAN İLAÇ TEMİNİ VE KULLANIMI KILAVUZU
Amaç
MADDE 1- (1) Bu Kılavuz, ülkemizde ruhsatlandırılmamış ve/veya ruhsatlandırıldığı hâlde çeşitli sebeplerle piyasada bulunmayan beşeri tıbbi ürünlerin, hastalıkların teşhis ve tedavisinde kullanılmak üzere yurt dışından reçete bazında veya acil durumlarda toplu temini ile söz konusu ürünlerin bilimsel veriler doğrultusunda tıbbi, etik, hukukî ve akılcı kullanımını sağlamak ve bu süreçteki usûl ve esasları belirlemek amacıyla hazırlanmıştır.
Dayanak
MADDE 2 -(1) Bu Kılavuz; 11/10/2011 tarihli ve 663 sayılı Sağlık Bakanlığı ve Bağlı Kuruluşlarının Teşkilat ve Görevleri Hakkında Kanun Hükmünde Kararnamenin 27 nci, 40 ıncı maddeleri, 14/5/1928 tarihli ve 1262 sayılı İspençiyari ve Tıbbi Müstahzarlar Kanununun Ek 7 nci maddesine ve Sağlık Uygulama Tebliği’nin 4.3 üncü maddesine istinaden hazırlanmıştır.
Kapsam
MADDE 3 -(1) Bu Kılavuz, ülkemizde ruhsatlandırılmamış ve/veya ruhsatlandırıldığı hâlde çeşitli sebeplerle piyasada bulunmayan beşeri tıbbi ürünlerin, hastalıkların teşhis ve tedavisinde kullanılmak üzere yurt dışından reçete bazında veya acil durumlarda toplu temini ile söz konusu ürünlerin bilimsel veriler doğrultusunda tıbbi, etik, hukukî ve akılcı kullanımını kapsar.
(2) İlaç, biyolojik ve tıbbi ürün klinik araştırmalarında kullanılan ürünlerin temini ve kullanımını kapsamaz.
Tanımlar
MADDE 3 -(1) Bu Kılavuzda yer alan;
a) Bakanlık: Sağlık Bakanlığını,
b) Kurum: Türkiye İlaç ve Tıbbi Cihaz Kurumunu,
c)Yurt dışı ilaç kullanımı: Ülkemizde henüz ruhsatlandırılmamış ve/veya ruhsatlandırıldığı hâlde çeşitli sebeplerle piyasada bulunmayan ilaçların, hastalıkların teşhis ve tedavisi amacıyla yurt dışından getirtilerek kullanımını,
ç) Acil Durum: Ani gelişen hastalık, kaza, yaralanma ve benzeri durumlarda olayın meydana gelmesini takip eden ilk 24 saat içinde tıbbi müdahale gerektiren durumlar ile ivedilikle tıbbi müdahale yapılmadığı veya başka bir sağlık kuruluşuna nakli halinde hayatın ve/veya sağlık bütünlüğünün kaybedilme riskinin doğacağı kabul edilen durumları,
d) FDA: Amerikan Gıda ve İlaç Kurumu’nu (U.S. Food and Drug Administration)
e) EMA: Avrupa İlaç Kurumu’nu (European Medicines Agency)
f) PIC/s: İlaç Denetim Sözleşmesi ve İlaç Denetim İşbirliği Programını (Pharmaceutical Inspection Convention and Pharmaceutical Inspection Cooperation Scheme)
g) SGK: Sosyal Güvenlik Kurumu’nu
ğ) TEB: Türk Eczacıları Birliği’ni
ifade eder.
Genel Hükümler
MADDE 4 -(1) Herhangi bir hastalığın tedavisinde, güncel tedavi rehberleri doğrultusunda etkililiği ve güvenilirliği bilimsel ve yeterli sayıda klinik çalışmalar ile kanıtlanmış, ilgili endikasyonda standart dozu belirlenerek Kurumca ruhsatlandırılmış beşeri tıbbi ürünlerin eczanelerden temin edilerek kullanımı esastır.
(2) Ancak ülkemizde ruhsatlandırılmamış ve/veya ruhsatlandırıldığı hâlde çeşitli sebeplerle piyasada bulunmayan ürünler, ülkemizdeki tedavi seçeneklerinin tümünü kullanmış veya kullanmasına engel durumu olan hastalar için hastalıklarının teşhis ve tedavisinde kullanılmasını gerektiren istisnai durumlarda TEB ve/veya SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından yurt dışından temin edilebilir. Bu ürünler TEB ve SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından sadece aşağıda tanımlanmış sıraya uyularak temin edilebilir:
a) FDA/EMA tarafından ruhsatlandırılmış ve piyasaya verilmiş olan veya PIC/s üyesi ülkelerde üretilen, ruhsatlandırılan ve piyasaya verilmiş olan beşeri tıbbi ürün temin edilmelidir.
b) (a) bendinde tanımlanan ülkelerde bulunamadığı veya temin edilemediği TEB ve/veya SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından Kuruma iletilen ürünlerin, (a) bendinde tanımlanan ülkeler dışında bir ülkede üretilen ve kullanılan ticari isimleri Yurt Dışı İlaç Listesine ilgili bilimsel komisyon görüşü alınarak Kurum Başkanı onayı ile eklenebilir.
(3) FDA/EMA tarafından ruhsatlandırılmamış olan beşeri tıbbi ürünlerin ticari isimlerinin Yurt Dışı İlaç Listesi’ne eklenmesi maksadıyla TEB ve/veya SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından Kuruma yapılacak olan başvuru sırasında aşağıda belirtilen belgeler sunulmalıdır:
a) İlgili beşeri tıbbi ürüne ait CPP (Certificate of Pharmaceutical Product) belgesi,
b) Ürün bilgileri (güvenlik bilgileri dahil) ve kullanıldığı ülke bilgilerini içeren üretici firmadan alınmış yazı veya kurumsal e-posta.
c) (a) ve (b) bentlerinde belirtilen belgelerin TEB ve SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından temin edilemediğinin kanıtlarıyla Kuruma iletildiği durumlarda ürün bilgilerine (güvenlik bilgileri dahil) ilişkin yurt dışı tedarikçi depodan alınmış yazı veya kurumsal e-posta.
(4) İkinci fıkra kapsamında yurt dışından temin edilen beşeri tıbbi ürünlerin üretim yerlerinin Kurum tarafından yapılan GMP denetimine ve ilaçların kalite kontrolüne yönelik analiz süreçlerine dolayısıyla ruhsatlandırma ve kalite kontrol süreçlerine tabi olmadığı hastanın hekimi tarafından hastalara anlatılmalıdır. Hekimi tarafından bilgilendirildiğine dair hastadan veya kanuni temsilcisinden rızasını belirten “Bilgilendirilmiş Hasta Olur Formu”(Ek-3)alınmalıdır.
(5) TEB ve/veya SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından temin edilebilecek ticari ilaç isminin bu maddenin ikinci fıkrasındaki kurallara göre belirlenmesi ve yurt dışından Ek-7 de belirtilen kurallara uygun olarak temin edilerek talep eden hekime/hastaya ulaştırılması gereklidir.
(6) TEB ve SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu bu kapsamda temin ettikleri beşeri tıbbi ürünlerin, temininden hastaya ulaşımına kadar geçen süreçlerin iyi dağıtım uygulamalarına göre gerçekleştirilmesinden sorumludur.
Yurt Dışı İlaç Listesi
MADDE 5 -(1) Kurum resmî internet sitesinde yayımlanan Yurt Dışı İlaç Listesinin “Aktif Etkin Madde Listesi” sekmesinde(Ek-1)yer alan beşeri tıbbi ürünlerin reçete bazında yurt dışından ithali için ayrıca Kurum ithalat izni aranmaz. Ancak, Yurt Dışı İlaç Listesinin “Aktif Etkin Madde Listesi” sekmesinde(Ek-1)“Sadece Kurumun Yazılı Onayı ile İthal Edilebilecek İlaçlar” başlıklı kolonda “1” ile işaretlenmiş ürünlerde ise her ithalat için Kurumdan hasta bazında ithalat izni alınmak zorundadır. Ayrıca "Reçete Türü" başlıklı kolonda “Kırmızı” ve “Yeşil” olarak belirtilen ilaçlarda ise Kurum Farmakovijilans ve Kontrole Tabi Maddeler Dairesi’ne her ithalat için Kontrole Tabi Maddelerin İthaline Mahsus Ruhsatname alınmasına ilişkin başvuru yapılması zorunludur.
(2) Yurt Dışı İlaç Listesinde(Ek-1)olmayan bir etkin madde reçete edilmiş ise ilgili etkin maddenin yurt dışından ithali için Kurum onayı şarttır.
a) Kurum tarafından etkin maddenin ithalatına onay verildiği takdirde ilgili etkin madde Yurt Dışı İlaç Listesi “Aktif Etkin Madde Listesi” sekmesine(Ek-1)ilave edilir.
b) Kurum tarafından ithaline izin verilen etkin maddenin hangi ticarî isimle ithal edilebileceğine yönelik piyasa araştırması TEB ve/veya SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından yapılır. TEB ve/veya SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından 4 üncü maddenin ikinci ve üçüncü fıkrasına uygun olarak belirlenen ve gerekli belgeler ile birlikte Kuruma resmi olarak iletilen beşeri tıbbi ürün isimleri Kurum tarafından Yurt Dışı İlaç Listesi “Tedarik Edilebilen İlaç Listesi” sekmesine (Ek-1) bilgi amaçlı olarak eklenir.
c) Kurum tarafından ithaline onay verilen etkin maddelere ait bilgileri içeren Yurt Dışı İlaç Listesi(Ek-1)her hafta Cuma günü mesai bitimine kadar güncellenerek Kurum resmî internet sitesinde yayımlanır.
ç) Başvurulara ayrıca yazılı olarak cevap verilmez. Listenin güncellenmesine kadar geçen süreyi bekleyemeyecek olan beşeri tıbbi ürün kullanım ve ithalat izin başvuruları bu kapsamda değerlendirilmez.
d) Reçete arkasına herhangi bir onay işlemi yapılmaz.
(3) Reçete, hastanın takip ve tedavisini üstlenen hekimin imza ve kaşesini taşır.
(4) Yurt Dışı İlaç Listesi “Aktif Etkin Madde Listesi” sekmesinde(Ek-1)olmayan ve ilk defa reçete edilen beşeri tıbbi ürünün kullanımı maksadıyla Kuruma yapılacak başvuru için gerekli belgeler:
a)“Yurt Dışı İlaç Kullanımı Talep Formu” (Ek-2)
b) Sağlık Kurulu Raporu veya İlaç Kullanım Raporu örneği,
c) Hasta tarafından okunarak imzalanmış genel“Bilgilendirilmiş Hasta Olur Formu” (Ek-3)
ç) İlgili beşeri tıbbi ürünün ilgili endikasyonda kullanımında etkililiği ve güvenilirliği ile alâkalı kanıt düzeyi yüksek olan bilimsel literatür/literatürler,
d) Hastanın aldığı tedavileri, bu tedavilerle elde edilen yanıtları ve tanıyla ilgili güncel laboratuvar değerlerini içeren epikriz,
(5) İkinci fıkra kapsamında yazılı olarak iletilecek başvurular“Sağlık Bakanlığı Türkiye İlaç ve Tıbbi Cihaz Kurumu, Söğütözü Mahallesi 2176. Sokak No:5 P.K. 06520 Çankaya/ANKARA”adresine yapılır.
(6) Bu maddenin birinci fıkrası kapsamında ithal edilen etkin maddelerin kullanımı için de hekim hastanın rızasını (yazılı onay) almak zorundadır.
Sağlık Uygulama Tebliğine göre bedeli talep edilecek yurt dışı ilaçlar
MADDE 6 -(1) Ülkemizde onaylı endikasyonu dâhilinde ilaçla tedavisi mümkün olan hastalıklar için yurt dışı ilaç kullanımına izin verilmez. Ancak, bilimsel veriler doğrultusunda belirgin avantaj sağlayan tedavi seçenekleri olması durumunda, yurt dışı ilaç kullanım talebi Kurum tarafından değerlendirilir. Yurt Dışı İlaç Listesi “Aktif Etkin Madde Listesi” sekmesinde(Ek-1)endikasyon belirtilen etkin maddelerin o endikasyonlarda kullanımı ve geri ödemesi için ayrıca Kurum izni aranmaz. Bu nedenle Kuruma yapılacak başvurular değerlendirmeye alınmaz.
(2) Başvurular, hastanın takip ve tedavisini üstlenen hekimin imza ve kaşesini taşır. Hasta, hasta yakını, eczacı veya başka şahıslarca başvuru formları düzenlenemez.
(3) Kurum tarafından, başvuruda kullanımı talep olunan beşeri tıbbi ürünün ilgili endikasyonda kullanımının bilimsel yönden uygun olup olmadığı değerlendirilir ve ancak uygunluk onayından sonra kullanılabilir. İş bu madde kapsamında Kurum izni alınmadan yurt dışı ilaç kullanımına başlanılmış ise geriye dönük bu gibi durumlar için yapılacak başvurular değerlendirilmeye alınmaz.
(4) Yurt Dışı İlaç Listesi “Aktif Etkin Madde Listesi” sekmesinde(Ek-1)endikasyon belirtilmeyen ya da belirtilen endikasyonlara uymayan ya da ilk defa reçete edilen ve geri ödemesi talep olunan beşeri tıbbi ürünün kullanımı maksadıyla Kuruma yapılacak başvuru için gerekli belgeler:
a)“Yurt Dışı İlaç Kullanımı Talep Formu”(Ek-2)
b) Sağlık Kurulu Raporu veya İlaç Kullanım Raporu örneği,
c) Hasta tarafından okunarak imzalanmış genel“Bilgilendirilmiş Hasta Olur Formu” (Ek-3)
ç) Bazı ilaçlar için özel hazırlanmış“Bilgilendirilmiş Hasta Olur Formu”ve özel belgeler(Ek-3A-E, Ek-5, Ek-6, Ek-9)
d) İlgili ürünün ilgili endikasyonda kullanımında etkililiği ve güvenilirliği ile ilgili kanıt düzeyi yüksek olan bilimsel literatür/literatürler,
e) Hastanın aldığı tedavileri, bu tedavilerle elde edilen yanıtları ve tanıyla ilgili güncel laboratuvar değerlerini içeren epikriz,
(5) Bu madde kapsamında yazılı olarak iletilecek başvurular“Sağlık Bakanlığı Türkiye İlaç ve Tıbbi Cihaz Kurumu, Söğütözü Mahallesi 2176. Sokak No:5 P.K. 06520 Çankaya/ANKARA”adresine yapılır.
(6) Uygulanan tedavi sonrası etkililik ve yan etki bakımından olumlu cevap alınan hastalarda tedaviye devam etmek istenir ise iznin son bir ayı içinde başvuru yapılabilir. Başvuruda hekim tarafından yeniden“Yurt Dışı İlaç Kullanım Talep Formu” (Ek-2)doldurulmayacak;“Bilgilendirilmiş Hasta Olur Formu (Ek-3) ” ve “Etkililik ve Yan Etki Geri Bildirim Formu (Ek-4) ”doldurulması yeterli olacaktır.
(7) Kurum, talep edilen beşeri tıbbi ürünün özelliğine göre ek form veya belge isteyebilir; gerektiğinde hastalıkla ilgili olarak yapılmış özel laboratuvar tetkiklerinin sonuçlarını da talep edebilir. (Kemik iliği biyopsisi, histopatoloji değerlendirme sonuçları ve benzeri)
(8) Hastalığın ilerlemesi, hastanın hayatını kaybetmesi, ilaç alerjisi ve ciddi advers etkiler gibi olumsuz bir durum gelişmesine bağlı olarak tedavinin sonlandırılmasını gerektiren hallerde en geç 5 (beş) iş günü içinde Kuruma tedaviyi üstlenen hekim tarafından gerekçesiyle birlikte yazılı bilgi verilmesi zorunludur.
(9) Uygun bulunmayan başvurular için hastanın hekimi tarafından bilimsel olarak geçerliliği bulunan itirazlar olması durumunda başvuru yeniden değerlendirilebilir.
(10) Yurt dışı etkin madde kullanım izni şahsî (hasta bazında) olup, hastanın içinde bulunduğu özel klinik durum için verilir. Herhangi bir hasta için verilen izin; benzer teşhis konulmuş fakat farklı klinik seyre sahip diğer hastalara emsal teşkil etmeyeceği gibi, Kurumun beşeri tıbbi ürünle ilgili genel bir sağlık stratejisini de yansıtmaz.
(11) Kurum, hastanın ilerleyen veya değişen klinik durumundan dolayı söz konusu izni iptal edebilir, doz ve uygulama süresinde değişiklik yapabilir.
Yurt dışı ilaç tedariki
MADDE 7 -(1) Yurt dışı ilaç listesinde(Ek-1)bulunan tüm beşeri tıbbi ürünler, TEB ve/veya SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu tarafından ithal edilebilir.
(2) TEB ve SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu, Yurt Dışı İlaç Listesi “Tedarik Edilebilen İlaç Listesi” sekmesinde(Ek-1)bulunan ürünleri stoklarında bulundurabilir.
(3) Yurt dışı ilaç listesi “Aktif Etkin Madde Listesi” sekmesinde bulunan etkin maddeyi içeren beşeri tıbbi ürünler ithal edilirken Kurum Bitkisel Destek ve İleri Tedavi Tıbbi Ürünleri Dairesinden ”İthalat Denetimi Tebliği” gereği Kontrol belgelerinin onaylarının alınması zorunludur.
(4) TEB ve SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu ithal ettikleri beşeri tıbbi ürünün kalite ve güvenliliğine ilişkin belgeleri 5 (beş) yıl süreyle saklamak zorundadır.
(5) TEB ve SGK bünyesindeki İbn-i Sina Sağlık Sosyal Güvenlik Merkezi ismindeki Ecza Deposu ithal ettikleri beşeri tıbbi ürün ticari isimlerini, bu ürünlerin kutu sayılarını ve kamuya açık kutu ücretlerini her üç ayda bir excel formatında e-posta ve resmi yazı yoluyla Kuruma iletir.
Yasaklar
MADDE 8-(1) Kurum tarafından verilmiş izinler doğrultusunda yapılan tedaviler ve bunlardan elde edilecek sonuçlar, Bakanlık dışında herhangi bir kurum/kuruluş ve/veya üçüncü kişiler ile paylaşılamaz, amacı dışında kullanılamaz. Bu kapsamda elde edilen veriler ile Kurum tarafından bilimsel yayın yapılabilir. Bunun haricinde herhangi bir kurum/kuruluş ve/veya üçüncü kişilerce bilimsel yayın amacıyla (vaka takdimi hariç) kullanılabilmesi için Kurum izni alınması zorunludur. Yine bu kapsamda elde edilen veriler ilaç ruhsatlandırma çalışmalarına esas veri olarak kullanılamaz. Gizlilik ilkelerine riayet etmeyenler hakkında ilgili mevzuat hükümleri doğrultusunda işlem yapılır.
Yürürlük
MADDE 9-(1) Bu Kılavuz onaylandığı tarihten itibaren yürürlüğe girer.
Yürütme
MADDE 10-(1) Bu Kılavuz hükümlerini Türkiye İlaç ve Tıbbi Cihaz Kurumu Başkanı yürütür.
Ekler;
Ek-2_Yurt_Dışı_ İlaç_Kullanım_Talep_Formu
Ek-3_Bilgilendirilmiş_Hasta_Olur_Formu
Ek-3A_PNH_Hastalarında_Eculızumab_Kullanımı_Icın_BHOF
Ek-3B_aHUS_Hastalarında_Eculızumab_Kullanımı_Icın_BHOF
Ek-3C_Albumine_Baglı_Paklıtaksel_Kullanımı_Icın_BHOF
Ek-3Ç_Natalizumab_Tedavı_Baslangıcı_Icın_Hasta Bilgilendirme_Ve_Onam_Formu
Ek-3D_Natalizumab_Bilgilendirme_Ve_Onam_Formu_(24_Aydan_36_Aya_Kadar)
Ek-3E_Anakinra_Kullanımı_İçin_Bilgilendirilmiş_Hasta_Olur_Formu
Ek-3F_Zydelig(İdelalisib) İçin Bilgilendirilmiş Hasta Olur Formu
Ek-4_Etkililik_Ve_Yan_Etki_Geri_Bildirim_Formu
Ek-5_PNH_Hastalarında_Eculizumab_Asi_Sertifikası
Ek-6_aHUS_Hastalarında_Eculizumab_Asi_Sertifikası
Ek-7 (Değişik 02.05.2016)_Yurt_Dışından_İlaç_Temini_İçin_Tedarikçilerde_Aranan_Şartlar
Ek-8_Yurt_Dışından_İlaç_Temin_Edebilecek_Tedarikçiler
Ek-9_Anakinra_Etkin_Maddesi_İçeren_İlaçlar_İçin_Güvenlik_İzlem_Formu
Daha önce yürürlükte olan kılavuzlar;
18.07.2014 tarihliYurt Dışından İlaç Temini Ve Kullanımı Kılavuzu ve Ekleri içintıklayınız.
19.12.2014 tarihliYurt Dışından İlaç Temini Ve Kullanımı Kılavuzu ve Ekleri içintıklayınız.
31.07.2015 tarihli Yurt Dışı İlaç Temini Ve Kullanımı Kılavuzunda değişiklik yapılmasına dair kılavuz ve Ekleri içintıklayınız.
30.03.2017
Eczanede Bulundurulması Zorunlu İlaçlar Listesi (ESKİ LİSTE)
15.05.2017
ECZANELERDE BULUNDURULMASI ZORUNLU İLAÇLAR
-AMİNOFİLİN ENJ.
-ANTİHİSTAMİNİK ENJ. -OKSİJENLİ SU
-DİAZEPAM TAB.
-DİGOKSİN ENJ.
-FENOBARBİTAL TAB.
-FUROSEMİDE ENJ.
-İNSÜLİN KRİSTALİZE ENJ.
-İNSÜLİN NPH
-İSOSORBİT DİNİTRAT SUBLİNGUAL TAB.
-KORTİKOSTEROİD ENJ. -KLONOZEPAM TAB.
-KLORPROMAZİN ENJ.
-KALSİYUM ENJ.
-NİFEDİPİN TAB.
-NİTROGLİSERİN TAB./SPREY -TRİMETOBENZAMİD ENJ.
-MORFİN SÜLFAT TAB. (tüm farmasötik dozaj formları)
-KONTROLLÜ SALIM SAĞLAYAN MORFİN SÜLFAT FİLM TAB. (tüm farmasötik dozaj formları)
BÜYÜK HACİMLİ PARANTERAL SOLÜSYONLAR
-%0,9 İZOTONİK SODYUM KLORÜR
-%5 DEKSTROZ SOLÜSYONU
-MULTİPL ELOKTROLİD SOLÜSYONU
-DEKSTRAN 40/70
ECZANELERDE BULUNDURULMASI ZORUNLU TIBBİ MALZEME
-BEDEN DERECESİ
-BRANÜL
-ELASTİK BANDAJ
-FLASTER
-KELEBEK SET
-SARGI BEZİ
-SERUM SETİ
-STERİL GAZ KOMPRES
-STERİL ENJEKTÖR (TEK KULLANIMLIK)
-SONDA (KADIN ERKEK EN AZ 3 DEĞİŞİK NUMARA)
 Eczanelerde Bulundurulması Zorunlu Tıbbi Malzemeler Hakkında
Eczanelerde Bulundurulması Zorunlu Tıbbi Malzemeler Hakkında
Teb Haberleri 14 Haziran 2017
15.05.2017
Vergi Borç Durumu Alma - İnternet Vergi Dairesi
1. Vergi Borç Durumunu gösterir belge almak için https://intvrg.gib.gov.tr adresine girilir.
2. Açılan sayfada Kullanıcı Girişi bağlantısı açılır.
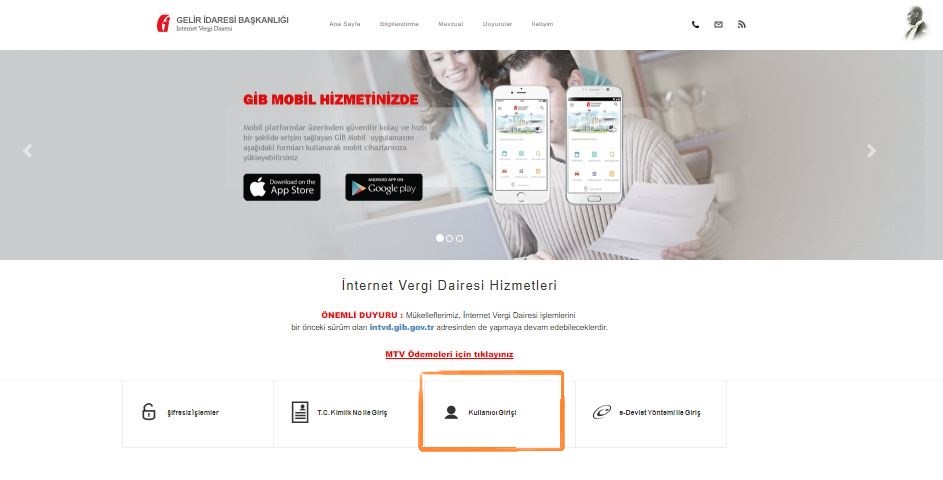
3. Vergi Dairenizden almış olduğunuz Kullanıcı Kodu, Parola ve Şifre ile kullanıcı girişi yapılır.
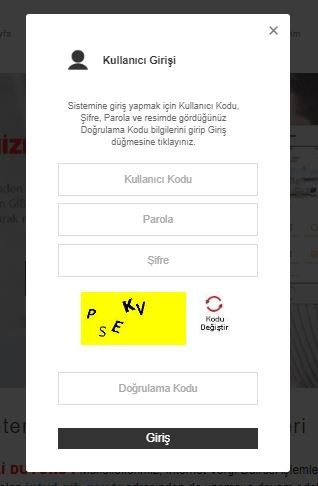
4. Mükellef İşlemleri'nden Dilekçeler seçilir.

5. Borcu Yoktur Talebi'ne basarak gerekli alanlar doldurulur. Girilen mail adresine en kısa sürede cevap mailı gelecektir.
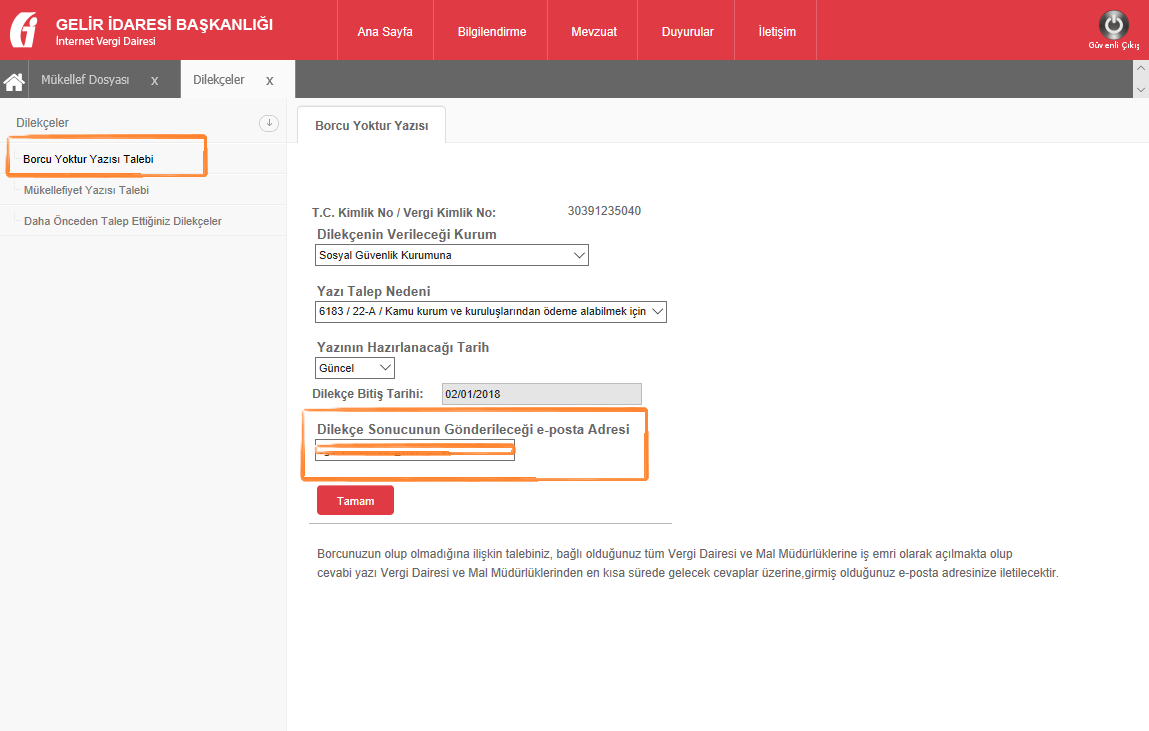
6. İşlem tamamlandıktan sonra en kısa sürede cevap mailı belirttiğiniz mail adresine cevap gelecektir.


03.01.2018
Türk Eczacıları Birliği Yardımlaşma Sandığı
Devlet Memurlarının aylıklarının hesaplanmasında esas olan katsayının 01.07.2018 – 31.12.2018 dönemi için (0,11794) olduğu, Maliye Bakanlığı Bütçe ve Mali Kontrol Genel Müdürlüğü 04.07.2018/ 27998389-010.06.02-5278 sayılı genelgesiyle 25.08.2017 tarihli ve 30165 sayılı Resmi Gazetede yayımlanmış olan Kamu Görevlilerinin Geneli ve Hizmet Kollarına Yönelik Mali ve Sosyal Haklara İlişkin 2018 ve 2019 Yıllarını Kapsayan 4.Dönem TopluSözleşmenin İkinci Kısım İkinci Kısım Birinci Bölümünün 5 inci maddesinin beşinci fıkrasında yer alan hükümlere istinaden, 657 sayılı DevletMemurları Kanununun 154 üncü maddesi uyarınca;
01.07.2018 – 31.12.2018 döneminde;
Giriş Aidatı: Kamuda Çalışmayan Eczacılar İçin: 176,91.-TL
Yıllık Aidat: Kamuda Çalışmayan Eczacılar İçin: 176,91.-TL.
Giriş Aidatı: Kamu Eczacısı için: 88,46.-TL.
Yıllık Aidat: Kamu Eczacısı için: 88,46.-TL. olarak tahsil edilecektir.
Her türlü tabii afetlerde zarar gören meslektaşlarımıza yapılacak yardıma kaynak olması amacıyla alınan afet fonu katkı paylarının "Türk Eczacıları Birliği Yardımlaşma Sandığı Afet Fonu Hesabı"na yatırılması hususunda Türk Eczacıları Birliği 39.Olağan Büyük Kongresi'nde karar alınmıştır.
39.Olağan Büyük Kongre'de afet fonu katkı payının oda aidatı kadar alınması kararlaştırılmıştır.
01.07.2018 – 31.12.2018 döneminde:
Afet Fonu: 58,97.-TL.
TEB Yardımlaşma Sandığı Banka Hesap Numaraları:
T.İş Bankası Farabi Şb. IBAN No: TR 81 0006 4000 0014 2400 0971 46 (Aidatlar)
T.İş Bankası Farabi Şb. IBAN No: TR 55 0006 4000 0014 2400 4427 40 (Afet Fonu)
Akbank T.A.Ş. Çankaya Şb. IBAN No: TR 12 0004 6008 6488 8000 0680 80 (Aidatlar)
|
DİKKAT EDİLECEK KONULAR |
|
|
|
*Yardımlaşma Sandığı hesaplarına banka aracılığıyla para yatırılırken dekont açıklamasına eczacı adı ve soyadının belirtilmesi, T.C. Kimlik numarasının yazılması *Kredi kullanmak isteyen üyelerimizin aidat ödemelerini mutlaka banka hesaplarımıza yatırmaları, *Afet fonu ödemelerinin mutlaka Afet Fonu hesabımıza yatırılması gerekliliğine özen göstermeleri, Yardımlaşma Sandığı banka hesaplarına yapılan havale ve EFT masrafa tabi değildir. KREDİ KULLANIMI |
|
1-Yardımlaşma Sandığı tarafından hazırlanan ve web sayfamızda da yayımlanan kredi talep formunun borçlu ve kefil eczacı tarafından eksiksiz tamamlanması, ıslak imza ile imzalanması ve bu evrakın aslı, oda onay yazısının aslı ile birlikte Sandığa ulaştırılması, (evrak üzerindeki karalama, daksil kullanımı gibi nedenlerle resmi evrak niteliği bozulan evrakların Sandığa gönderilmemesi) 2-Kredi kullanmak isteyen üyelerimizin munzam eksiği varsa tamamlayarak ilgili banka dekontunun kredi talep formuna eklenmesi, 3-Yardımlaşma Sandığımızca kontrol edilen ve kullandırılması uygun görülen krediler için Türkiye İş Bankası A.Ş.’ye Kredilendirme Talimatı gönderilecektir. Kredi kullanacak Üyemiz kredi kullanmak istedikleri şube tarafından bilgilendirileceklerdir. 4-Kredi kullanacak üyemiz ile kefilibanka şubesine giderek ilgili sözleşmeyi imzalayarak krediyi alabileceklerdir. 5-Kefil ile borçlunun farklı şehirlerde olması durumunda, önce kefil bulunduğu ilde banka şubesinde sözleşmeyi imzalayacak ardından banka, dahili kargo ile sözleşmeyi kredi kullanacak eczacının şubesine ulaştıracaktır. YARDIMLAR VEFAT YARDIMI |
KARŞILIKSIZ SOSYAL YARDIM
|
|
AFET YARDIMI |
|
TÜRK ECZACILARI BİRLİĞİYARDIMLAŞMA SANDIĞI YÖNETMELİĞİ
BİRİNCİBÖLÜM
Amaç, Kapsam, Hukuki Dayanak ve Tanımlar
Amaç
Madde 1-Bu Yönetmeliğin amacı, Türk Eczacıları Birliği Yardımlaşma Sandığının yönetimi, çalışması, giriş ve yıllık aidatları ile yapılacak yardımlarla ilgili usul ve esasları belirlemek, görev, yetki ve sorumluluklarını düzenlemektir.
Kapsam
Madde 2-Bu Yönetmelik 6643 sayılı yasanın l inci maddesinde belirtildiği gibi Türk Eczacıları Birliğine kayıtlı olan tüm eczacıları kapsar.
Hukuki Dayanak
Madde 3-Bu Yönetmelik 6643 sayılı yasanın 4078 sayılı kanun ile değişik 58fnci maddesine göre hazırlanmıştır.
Tanımlar
Madde 4-Bu Yönetmelikte geçen
TEB : Türk Eczacıları Birliğini
Sandık : Türk Eczacıları Birliği Yardımlaşma Sandığı’nı
Sandık Yönetimi : Türk Eczacıları Birliği Yardımlaşma Sandığı’nı yönetmekle
görevli olan Türk Eczacıları Birliği Merkez Heyeti’ni
Üye : 6643 Sayılı Yasanın 58fnci maddesi uyarınca Sandığa üye
olmak zorunda olan eczacıları ifade eder.
İKİNCİBÖLÜM
Yardımlaşma Sandığıfnın Amaçları ve Üyelik Koşulları
Sandığın Amaçları
Madde 5-Yardımlaşma Sandığıfnın amaçları aşağıda belirtilmiştir.
a) Sandık üyelerinin tasarrufta bulunmasını sağlamak,
b) Sandık üyesi olan eczacıların, sosyal ve ekonomik çıkarlarını koruyup geliştirici çalışmalarda bulunmak,
c) Ölüm, hastalık, muhtaçlık, afet ve benzeri hallerde üyelerine yardımda bulunmak,
d) Sandık üyesi eczacılar arasında sosyal ve ekonomik dayanışmayı güçlendirmek.
Sandığa Üye Olmak
Madde 6-(Değişik:RG-23/5/2016-29720)
6643 sayılı Kanunun 58 inci maddesine göre Türk Eczacıları Birliğine kayıt olurken Yardımlaşma Sandığına kayıt zorunluluğu bulunmayıp, isteğe bağlı olarak üye olunabilir.
Üyelik Sıfatının Sona Ermesi
Madde 7-Aşağıda belirtilmiş bulunan hallerde üyelik sıfatı sona erer:
a)(Değişik:RG-23/5/2016-29720)Oda ve/veya sandık kaydının silinmesi suretiyle,
b) Ölüm.
Yukarıdaki nedenlerle üyeliğin sona ermesi halinde üyelerin birikmiş paralarından varsa borçları düşürüldükten sonra kalan miktar üyeliğin sona erdiği tarihten itibaren iki ay içinde üyeye hak ettiği yasal birikimleriyle iade edilir. Üyelik ölüm ile sona ermişse, yukarıda belirtilen şekilde mirasçıları hak sahibidir.
Yeniden Üye Olmak
Madde 8-Oda kaydının silinmesi suretiyle üyelikten ayrılanlar daha sonra yeniden Sandık üyesi olduklarında eski üyelikleri sırasında kazandıkları kıdem ve haklar dikkate alınmaz.
ÜÇÜNCÜ BÖLÜM
Yardımlaşma Sandığının Yönetimi, Çalışma Usulleri,
Görev, Yetki ve Sorumlulukları
Sandığın Yönetimi
Madde 9-Sandığın Yönetimi Türk Eczacıları Birliği Merkez Heyetinin görevleri içindedir. Bu nedenle Sandık Türk Eczacıları Birliği Merkez Heyetince yönetilir ve Türk Eczacıları Birliği Merkez Heyeti Denetleme Kurulu tarafından denetlenir.
Sandık Yönetim Çalışma Usulleri
Madde 10-Sandığı yönetmekle görevli olan Türk Eczacıları Merkez Heyetinin 6643 Sayılı yasada ve bu yasaya bağlı olarak çıkarılan Türk Eczacıları Birliği Yönetmeliğinde belirtilen çalışma usulleridir.
Sandık Yönetiminin Görev ve Yetkileri
Madde 11-Sandık yönetiminin görev ve yetkileri aşağıda belirtilmiştir.
a) Türk Eczacıları Birliği adına bu Yönetmeliğin 5fnci maddesinde belirtilen amaçları gerçekleştirmek,
b) Sandığın amacına uygun olarak Türk Eczacıları Birliği adına gayrimenkuller
satın almaya, kiralamaya veya inşa ettirmeye, uhdesinde bulunan gayrimenkulleri bedelleri ve maksatlara tahsis edilmek üzere satmaya, bunlar üzerinde ayni haklar tesisine, ikraz ve istikrazda bulunmaya, sandık lehine her türlü kararlar almaya Sandık Yönetimi yetkilidir.
c) Sandığın idaresi için lüzumlu personeli istihdam ile bu hususta gerekli masraflar yapmak,
d) Gerekli gördüğü hallerde danışmanlar atamak, komisyonlar oluşturmak,
e) Türk Eczacıları Birliği Büyük Kongresinde Sandık ile ilgili alınan kararları yürütmek,
f) Sandıkça yapılacak bağışların, yardımların ve tahsislerin miktarlarını
belirlemek,
g) Sandık üyesi eczacılar arasında sosyal ve ekonomik dayanışmanın
güçlendirilmesi hususunda uygulama biçimlerini belirlemek,
h) Gerekli görülen illerde şubeler ve/veya temsilcilikler açmak,
i) Ayrı bir karar defteri tutarak, Sandık ile ilgili aldığı kararları üyelerine duyurmak,
j) Sandık yönetmeliğinde gerekli gördüğü değişiklik tekliflerini Türk Eczacıları Birliği Büyük Kongresinin onayına sunmak,
k)(Değişik:RG-23/5/2016-29720)Sandığın gelir ve giderleri ile ilgili kayıtları tutmak,
l) (Ek bent: R.G 14 Temmuz 1998 / 23402)Büyük Kongrede alınan karar
doğrultusunda emeklilik işlemlerinin düzenlenmesini ve yürütülmesini
sağlamak.
Sorumluluk
Madde 12-Sandığı Yönetmekle görevli olan Türk Eczacıları Birliği Merkez Heyetinin faaliyetleri açısından Türk Eczacıları Birliği Büyük Kongresine karşı sorumludur. Sandık çalışmaları Türk Eczacıları Merkez Heyetinin çalışma raporu içerisinde ayrı bir bölüm halinde gösterilir ve Sandık çalışma raporu ile Sandık bilançosu ayrı bir gündem içerisinde Büyük Kongreye sunulur.
DÖRDÜNCÜ BÖLÜM
Yardımlaşma Sandığı Gelir, Gider, Hesap ve Yardımları
Gelirler
Madde 13-Yardımlaşma Sandığının gelirleri aşağıda belirtildiği gibidir.
a) Giriş ve Yıllık Aidatlar
b) Diğer Gelirler
Girişve Yıllık Aidatlar
Madde 14- (Değişik:RG-23/5/2016-29720)
Sandığa üye olacak eczacı bir defaya mahsus olmak üzere üye kaydı sırasında kayıtlı olduğu eczacı odasına o yıl için ödeyeceği yıllık aidatın üç katını giriş aidatı olarak Yardımlaşma Sandığına öder. Yıllık aidat, üyenin kayıtlı olduğu eczacı odasına o yıl için ödeyeceği oda yıllık aidatının üç katıdır. Üyelere duyurulan yıllık aidatların aynı yılın Şubat ayı sonuna kadar Sandık yönetiminin belirleyeceği şekilde Sandığa ödenmesi zorunludur. Sandığa ait o yılki yıllık aidatlarını ödemeyen üyeler hakkında 9/6/1932 tarihli ve 2004 sayılı İcra ve İflas Kanunu hükümlerince bağlı bulundukları Oda tarafından yasal işlem yapılır.
Diğer Gelirler
Madde 15-Amacın gerçekleştirilmesi sonucu elde edilecek her türlü gelir, diğer gelirleri teşkil eder.
Giderler
Madde 16-Sandığın yönetim ve personel giderleri ile amaçlar doğrultusunda yapılan bağışlar, yardımlar ve tahsisler ile benzeri giderler Sandığın giderlerini teşkil eder.
Hesaplar
Madde 17-Sandığın Hesapları ayrıca tutulur ve Türk Eczacıları Birliği Merkez Heyetinin bilançosu içinde ayrı bir bölüm halinde gösterilir.
Yardımlar
Madde 18-Verilme biçimleri ile limitleri Sandık Yönetimi tarafından her takvim yılı için belirlenen ve üyelere duyurulan yardımlar şunlardır:
a) Ölüm Yardımı
b) Muhtaçlık Yardımı
c) Afet Yardımı
Ölüm Yardımı
Madde 19-Üyenin ölümü halinde yapılan yardımdır. Varsa ölen üyenin noter kanalıyla Sandığa bildirdiği kimseye, yoksa veraset ilamı gereğince mirasçılarına yapılır. Madde 7fde belirtildiği şekilde tahsil edilemeyen borçları varsa, bu miktar ölüm yardımından düşülür. Haklarında yapılan kanuni takibata rağmen üç senedir Sandığa olan borcu tahsil edilememiş üyeye ölüm yardımı yapılmaz. Üyenin kimsesi yoksa cenazesi birinci sınıf törenle Sandık tarafından kaldırılır ve kabri yaptırılır.
Muhtaçlık Yardımı
Madde 20-Üyenin bağlı olduğu eczacı odası tarafından bildirilmek şartıyla Sandık Yönetimince kabul edilebilecek bir ihtiyaç nedeniyle yapılan yardımdır.
Afet Yardımı
Madde 21-Üyenin ya da işyerinin maruz kaldığı deprem, sel, seylap, dahili ya da harici su basması, yangın, yer kayması ve bu gibi elde olmaksızın meydana gelen durumlarda yapılan yardımdır.
Sosyal ve Ekonomik Dayanışma
Madde 22-Sandık üyeleri arasında sosyal ve ekonomik dayanışmayı güçlendirmek amacıyla kimlere, ne şekilde yardım yapılacağı ve karşılığının ne şekilde geri alınacağı Sandık Yönetimince belirlenir ve üyelere düzenli bir biçimde duyurulur.
Bağışve Yardımların Miktarı
Madde 23-Bu Yönetmelikte belirtilen bağışların, yardımların ve tahsislerin miktarlarını ve verilme koşullarını belirlemeye Sandık Yönetimi yetkilidir.
Yardımlar için Başvuru Süresi
Madde 24-Üye veya hak sahipleri kendilerine yardım yapılmasını gerektirecek halin oluşmasından itibaren bir yıl içerisinde başvuruda bulunmayıp gerekli belgeleri Sandık Yönetimine sunmadıkları taktirde haklarını kaybederler.
Yürürlükten Kaldırma
Madde 25-Bu Yönetmeliğin yürürlüğe girmesiyle 4 Ocak 1996 gün ve 22513 sayılı Resmi Gazetefde yayımlanan Türk Eczacıları Birliği Yardımlaşma Sandığı Yönetmeliği yürürlükten kalkmıştır.
BEŞİNCİBÖLÜM
Çeşitli Hükümler
Yürürlük
Madde 26-Bu Yönetmelik yayımı tarihinde yürürlüğe girer.
Yürütme
Madde 27-Bu Yönetmelik hükümlerini Türk Eczacıları Birliği Merkez Heyeti Başkanı yürütür.
03.09.2018
Türk Eczacıları Birliği Lisansüstü Karşılıklı Burs Yönergesi
TÜRK ECZACILARI BİRLİĞİ
LİSANSÜSTÜ KARŞILIKLI BURS YÖNERGESİ
1Amaç ve kapsam: Bu yönerge, Türk Eczacıları Birliği tarafından eczacılık fakültesi mezunlarının ülkemizin belirli alanlardaki eczacı insan gücü ihtiyacını karşılamak üzere yurtdışında burslu olarak lisans üstü eğitimi yapmasını düzenlemektir.
2-Tanımlar:
a)Burs veren: Türk Eczacıları Birliğini
b)Burs alan: Bu yönerge kapsamında burstan faydalanan kişiyi
c)Lisans üstü eğitim: Örgün yüksek lisans ve doktora eğitimini tanımlar.
d)Jüri: Her yıl bu kapsamda burs verilecek alanları ve kişileri seçen, Türk Eczacıları Birliği Merkez Heyetinin atayacağı kişilerden oluşan komitedir.
3Genel Koşullar:
3.1. Adaylarda aranan koşullar:
a)Eczacılık Fakültesi mezunu olmak,
b)Başvuru tarihinde yüksek lisans için 30, doktora için 35 yaşını aşmamış olmak,
c)Jüri tarafından yıllık olarak belirlenen ve ilan edilen programlardan kabul mektubu almış olmak,
d)Yüksek lisansa veya doğrudan doktoraya başvuracak adaylar için toplam mezuniyet ortalamasının (CGPA) 4’lü sistemde 3.00’ten az olmaması,
5) Yüksek lisansını Türkiye’de yapıp doktoraya başvuracak adaylar için toplam mezuniyet ortalamasının (CGPA) 4’lü sistemde 3.50’den az olmaması, 6) Yabancı dil puanının YDS 70 ve üzeri, TOEFL 6.5/8.00 olması.
3.2. Bursun kapsamı:
Burs, gidilen bölgeye / ülkeye göre miktarı TEB tarafından belirlenen aylık ücreti, en az üç ay önceden alınmak şartıyla yılda bir kez gidiş-dönüş uçak biletini kapsamaktadır. Pasaport, vize, harçlar ve diğer resmi işlemlerle ilgili giderler aday tarafından karşılanacaktır. İlgili üniversite harcının ne kadarının ödeneceği Jüri tarafından kararlaştırılacaktır.
3.3. Adaylardan istenen belgeler:
⦁2 adet transkript
⦁2 adet “Aslı gibidir” onaylı diploma örneği
⦁2 adet son altı ayda çekilmiş fotoğraf
⦁Niyet mektubu (2 sayfayı geçmeyecek şekilde)
⦁İlgili programlardan kabul mektubu
⦁İlgili programın müfredatı
⦁Dil puanını gösterir belge
⦁Üniversite yıllık harcının ne kadar olduğuna dair üniversiteden alınmış yazı
3.4. Bursların duyurulması
Yıllık burs alanları, başvuru son tarihi ve diğer özel koşullar Türk Eczacıları Birliği’nin resmi web sitesinden duyurulacaktır.
3.5. Burs alanların seçimi
Tüm belgelerini tamamlamış olan adayların başvuruları, Burs Jürisi tarafından yapılacak mülakatta değerlendirilecektir. Mülakat tarihi Türk Eczacıları Birliği resmi web sitesinde ilan edilecektir.
3.7. Burs alanın yükümlülükleri
1Yüksek lisans bursiyerleri azami 3, doktora bursiyerleri azami 7 yıl içinde programlarını tamamlamak zorundadır. Programı tamamlayamayan öğrencilerin bursu kesilir ve kendisine ödenen ücret ve diğer tüm harçların ödeme tarihinden itibaren işleyecek yasal faizi ile birlikte iadesi alınır.
2Programı tamamlayan bursiyer öncelikle Türk Eczacıları Birliği’nin personel ihtiyacı açısından değerlendirilecektir. İhtiyaç duyulan bursiyerler burs karşılığı olarak ve ücretli biçimde, en az burs alınan süre kadar istihdam edilecektir. Bursiyer, mezun olduktan sonra üç ay içinde gösterilen yerde (Ankara) göreve başlamak durumundadır. İhtiyaç duyulduğu halde Türk Eczacıları Birliği’nde çalışmayı kabul etmeyen bursiyer için yapılan tüm harcamaların iadesi alınır. Süre bitiminden önce işten ayrılan bursiyere kalan süre için yapılan tüm harcamaların ödeme tarihinden itibaren işleyecek yasal faizi ile birlikte iadesi alınır.
Şu kadar ki;
3-Bursiyer, Türk Eczacıları Birliği’nin personel ihtiyacı açısından değerlendirilip uygun bulunduğu halde, göreve başlama süresi içinde (3 ay) kendisi Türkiye sınırları içinde alanıyla ilgili başka bir iş bulursa, bu süreyi bu işyerinde geçirmeyi talep edebilir. Bu durumda bursiyer, Merkez Heyeti’nin uygun görüşünü alarak diğer işyerinde çalışabilir. Ancak çalışma yükümlülüğü süresince her işyeri değişikliğinde bu onayı almak zorundadır.
4-TEB’de burs karşılığı ya da herhangi bir işte çalışmıyor ise tam zamanlı çalışan ya da uygunluk belgesi ile başka bir işte çalışan değilse, her koşulda bursiyer, Türk Eczacıları Birliği’nin kendisine verdiği çeşitli proje, araştırma, eğitim vb. görevlerde eğitimini tamamladığı sürenin iki katı dönemde en az 2160 saat hizmet vermek durumundadır. Aksi takdirde verilen yapılan harcamalar yasal faiziyle birlikte ödemek zorundadır.
5-Bu koşulları yerine getirmeyen bursiyer, Türkiye’ye dönüş tarihinden itibaren en geç bir buçuk yıl içerisinde kendisine verilen burs ve diğer ücretleri ödeme tarihinden itibaren işleyecek yasal faizi ile birlikte, en geç bir yıl içerisinde ilk taksiti ödemek koşuluyla en fazla altı taksit halinde ödemeyi kabul ve taahhüt etmiş sayılır.
4.Burs verenin yükümlülükleri
1.Burs veren, burs alana yapılacak ödemeleri saptamak ve mücbir sebep halleri sayılamayacak durumlarda tam olarak taahhüt ettiği şekilde ödemekle yükümlüdür.
2.Burs veren, taahhüt ettiği aylık ödeme miktarını iki ay arka arkaya yahut bir yıl içinde üç kere ödemezse, burs alanın burs verene karşı yükümlülükleri ortadan kalkmış sayılır.
5.Çeşitli ve son hükümler
Bu yönetmelik ile düzenlenmemiş konularda Yüksek Öğretim Kurumu tarafından kullanılan benzer burs yönetmelikleri hükümleri esas alınıp geçerli sayılacaktır.
Burs alanla bu yönergeye bağlı sözleşmelerde uyuşmazlıkların çözümünde Türk hukuku geçerli olup, TÜRKİYE/ ANKARA mahkemeleri ve icra müdürlükleri yetkilidir.
6.Yürütme
Bu Yönerge hükümlerini Türk Eczacıları Birliği Merkez Heyeti yürütür.
23.10.2018
ECZANELERDE BULUNDURULMASI ZORUNLU İLAÇ VE TIBBİ MALZEMELER (08.11.2018)
08.11.2018 TARİHİNDE YAYIMLANAN GÜNCEL LİSTE ECZANELERDE BULUNDURULMASI ZORUNLU İLAÇ VE TIBBİ MALZEMELER
ANTİHİSTAMİNİK ENJ
ALPRAZOLAM TAB
DİAZEPAM TAB
FENOBARBİTAL TAB
FUROSEMİDE ENJ
İSOSORBİT DİNİTRAT SUBLİNGUAL TAB
KAPTORİL TAB.
KORTİKOSTEROİD ENJ
KLONOZEPAM TAB
LORAZEPAM TAB
MORFİN SÜLFAT TAB. İÇEREN MÜSTAHZARLARDAN EN AZ 1 FORM
NİFEDİPİN TAB
NİTROGLİSERİN TAB./ SPREY
OKSİJENLİ SU
%0,9 İZOTONİK SODYUM KLORÜR SOLÜSYONU
%5 DEKSTROZ SOLÜSYONU
ATEŞ ÖLÇER
BRANÜL
ELASTİK BANDAJ
FLASTER
KELEBEK SET
SARGI BEZİ
SERUM SETİ
STERİL GAZ KOMPRES
STERİL ENJEKTÖR (TEK KULLANIMLIK)
 Eczanelerde Bulundurulması Zorunlu İlaçlar ve Tıbbi Malzemelerin Günce...
Eczanelerde Bulundurulması Zorunlu İlaçlar ve Tıbbi Malzemelerin Günce...
09 Kasım 2018 devamı
09.11.2018

